- Định luật nhiệt động lực học là gì?
- Nguồn gốc của các định luật nhiệt động lực học
- Định luật đầu tiên của nhiệt động lực học
- Định luật thứ hai của nhiệt động lực học
- Định luật thứ ba của nhiệt động lực học
- Định luật 0 của nhiệt động lực học
Chúng tôi giải thích các định luật nhiệt động lực học là gì, nguồn gốc của các nguyên tắc này là gì và các đặc điểm chính của mỗi nguyên tắc đó.

Định luật nhiệt động lực học là gì?
Các định luật nhiệt động lực học (hoặc các nguyên tắc của nhiệt động lực học) mô tả hoạt động của ba đại lượng vật lý cơ bản, nhiệt độ, các Năng lượng vàSự hỗn loạn, đặc trưng cho các hệ thống nhiệt động lực học. Thuật ngữ "nhiệt động lực học" xuất phát từ tiếng Hy Lạp phích nước, Nó có nghĩa là gì "nhiệt", Y máy nổ, Nó có nghĩa là gì "lực lượng”.
Về mặt toán học, những nguyên tắc này được mô tả bởi một bộ phương trình giải thích hoạt động của các hệ nhiệt động lực học, được định nghĩa là bất kỳ đối tượng nghiên cứu nào (từ một phân tử hoặc một con người, cho đến khi bầu khí quyển hoặc đun sôi nước trong một cái chảo).
Có bốn định luật nhiệt động lực học và chúng rất quan trọng để hiểu được các quy luật vật lý của vũ trụ và không thể xảy ra một số hiện tượng như sự chuyển động vĩnh viễn.
Nguồn gốc của các định luật nhiệt động lực học
Bốn nguyên tắc của nhiệt động lực học Chúng có nguồn gốc khác nhau, và một số được tạo ra từ những công thức trước đó. Trên thực tế, cơ sở đầu tiên được thành lập là công trình thứ hai, là công trình của nhà vật lý và kỹ sư người Pháp Nicolás Léonard Sadi Carnot vào năm 1824.
Tuy nhiên, vào năm 1860, nguyên lý này được Rudolf Clausius và William Thompson đưa ra một lần nữa, sau đó bổ sung cái mà ngày nay chúng ta gọi là Định luật Nhiệt động lực học thứ nhất. Sau đó, định đề thứ ba xuất hiện, còn được gọi là "định đề Nerst" vì nó phát sinh nhờ các nghiên cứu của Walther Nernst từ năm 1906 đến năm 1912.
Cuối cùng, cái gọi là "định luật số không" xuất hiện vào năm 1930, do Guggenheim và Fowler đề xuất. Cần phải nói rằng không phải trong mọi lĩnh vực nó đều được công nhận là luật chân chính.
Định luật đầu tiên của nhiệt động lực học

Luật đầu tiên được gọi là "Định luật Bảo toàn Năng lượng" vì nó quy định rằng trong bất kỳ hệ thống cô lập với môi trường của nó, tổng lượng năng lượng sẽ luôn bằng nhau, mặc dù nó có thể được chuyển đổi từ một dạng năng lượng sang các dạng năng lượng khác nhau. Hay nói cách khác: năng lượng không thể được tạo ra hoặc bị phá hủy, chỉ được chuyển hóa.
Do đó, bằng cách cung cấp một lượng nhiệt nhất định (Q) cho một hệ vật chất, tổng lượng năng lượng của nó có thể được tính bằng nhiệt lượng cung cấp trừ điCông việc (W) được thực hiện bởi hệ thống đối với môi trường xung quanh nó. Được biểu thị bằng công thức: ΔU = Q - W.
Để làm ví dụ về định luật này, chúng ta hãy hình dung một động cơ máy bay. Nó là một hệ thống nhiệt động lực học bao gồm nhiên liệu phản ứng hóa học trong quá trình sự đốt cháy, giải phóng nhiệt và hoạt động (làm cho máy bay chuyển động). Vì vậy: nếu chúng ta có thể đo khối lượng công việc đã hoàn thành và nhiệt lượng tỏa ra, chúng ta có thể tính toán tổng năng lượng của hệ thống và kết luận rằng năng lượng trong động cơ không đổi trong suốt chuyến bay: năng lượng không được tạo ra cũng không bị phá hủy, thay vào đó nó đã thay đổi của năng lượng hóa học đến năng lượng calo YĐộng năng (chuyển động, tức là làm việc).
Định luật thứ hai của nhiệt động lực học
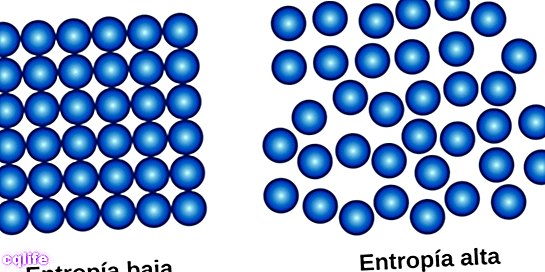
Định luật thứ hai, còn được gọi là «Định luật Entropy», có thể được tóm tắt trong đó số lượng của Sự hỗn loạn trong vũ trụ có xu hướng tăng thời tiết. Điều này có nghĩa là mức độ rối loạn của các hệ thống tăng lên cho đến khi đạt đến điểm cân bằng, đây là trạng thái mất trật tự lớn nhất của hệ thống.
Định luật này đưa ra một khái niệm cơ bản trong vật lý: khái niệm entropi (được biểu thị bằng chữ S), trong trường hợp các hệ thống vật lý biểu thị mức độ rối loạn. Nó chỉ ra rằng trong mọi quá trình vật chất mà có sự chuyển hóa của năng lượng, một lượng năng lượng nhất định không thể sử dụng được, tức là nó không thể làm việc. Nếu bạn không thể làm việc, trong hầu hết các trường hợp, năng lượng đó là nhiệt. Nhiệt lượng mà hệ thống giải phóng, những gì nó làm là làm tăng sự rối loạn của hệ thống, entropy của nó. Entropy là thước đo sự rối loạn của một hệ thống.
Việc xây dựng luật này thiết lập rằng sự thay đổi trong entropy (dS) sẽ luôn bằng hoặc lớn hơntruyền nhiệt (dQ), chia cho nhiệt độ (T) của hệ thống. Tức là: dS ≥ dQ / T.
Để hiểu điều này bằng một ví dụ, chỉ cần đốt một lượng nhất định vấn đề và sau đó thu thập tro kết quả. Khi cân chúng, chúng tôi sẽ xác minh rằng nó ít vật chất hơn những gì ở trạng thái ban đầu: một phần của vật chất đã được chuyển thành nhiệt ở dạng khí rằng họ không thể thực hiện công việc trên hệ thống và họ góp phần vào sự rối loạn của hệ thống.
Định luật thứ ba của nhiệt động lực học

Định luật thứ ba nói rằng entropy của một hệ thống được đưa về độ không tuyệt đối sẽ là một hằng số xác định. Nói cách khác:
- Khi đạt đến độ không tuyệt đối (không tính bằng đơn vị Kelvin), các quá trình của hệ thống vật lý dừng lại.
- Khi đạt đến độ không tuyệt đối (không tính bằng đơn vị Kelvin), entropi có giá trị nhỏ nhất không đổi.
Rất khó để đạt được cái gọi là độ không tuyệt đối (-273,15 ° C) hàng ngày, nhưng chúng ta có thể suy nghĩ về định luật này bằng cách phân tích những gì xảy ra trong tủ đông: món ăn mà chúng ta lắng đọng ở đó sẽ trở nên lạnh đến mức các quá trình sinh hóa bên trong nó sẽ chậm lại hoặc thậm chí dừng lại. Đó là lý do tại sao quá trình phân hủy của nó bị trì hoãn và sự tiêu thụ lâu hơn nữa.
Định luật 0 của nhiệt động lực học
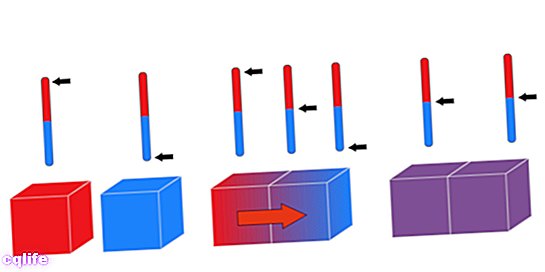
"Luật số không" được biết đến với cái tên đó mặc dù nó là luật cuối cùng được áp dụng. Cũng được biết đến như là Định luật cân bằng nhiệt, nguyên tắc này ra lệnh rằng: “Nếu hai hệ thống ở cân bằng nhiệt độc lập với hệ thứ ba, chúng cũng phải cân bằng nhiệt với nhau ”. Nó có thể được diễn đạt một cách logic như sau: nếu A = C và B = C thì A = B.
Định luật này cho phép chúng ta so sánh nhiệt năng của ba vật A, B và C. Nếu vật A ở trạng thái cân bằng nhiệt với vật C (chúng có cùng nhiệt độ) và B cũng có cùng nhiệt độ với C thì A và B có cùng nhiệt độ.
Một cách khác để phát biểu nguyên tắc này là lập luận rằng khi hai vật có nhiệt độ khác nhau tiếp xúc với nhau, chúng sẽ trao đổi nhiệt cho đến khi nhiệt độ của chúng bằng nhau.
Rất dễ tìm thấy các ví dụ hàng ngày về luật này. Khi chúng ta tiếp xúc với nước lạnh hoặc nước nóng, chúng ta sẽ nhận thấy sự khác biệt về nhiệt độ chỉ trong những phút đầu tiên vì cơ thể chúng ta sau đó sẽ đi vào trạng thái cân bằng nhiệt vớiNước uống và chúng tôi sẽ không còn nhận thấy sự khác biệt. Điều tương tự cũng xảy ra khi chúng ta bước vào phòng nóng hoặc lạnh: lúc đầu chúng ta sẽ nhận thấy nhiệt độ, nhưng sau đó chúng ta sẽ ngừng nhận thức sự khác biệt vì chúng ta sẽ đi vào trạng thái cân bằng nhiệt với nó.
